Tính kim loại giảm dần Li có tính kim loại mạnh nhất tính phi kim tăng dần F. Trong bảng tuần hoàn.
Nguyên nhân của sự biến đổi tuần hoàn tính chất của các nguyên tố là do sự biến đổi tuần hoàn của.

Sự biến thiên các nguyên tố trong bảng tuần hoàn. Nguyên tố X là phi kim có hoá trị cao nhất với oxi là. Đi từ trên xuống theo chiều tăng dần điện tích hạt nhân. Cấu chế tạo ra bảng tuần hoàn.
Sự biến đổi tuần hoàn về cấu hình electron. Trong 1 nhóm A. Các sự khác lạ chính giữa nguyên tắc quản trị và vận hành của Fayol và.
KIẾN THỨC CẦN NẮM VỮNG. Tính kim loại phi kim. Quy luật biến thiên tính chất các nguyên tố trong bảng tuần hoàn có thể tóm tắt như sau.
Bán kính nguyên tửĐộ âm điệnNăng lượng ion hóaTínhkim loạiTínhphi kimTính axit của oxit vàhiđroxitTính bazơ của oxit và hiđroxitTrong. Bạn trọn vẹn có thể lại Báo lỗi ở phía dưới để Admin được tương hỗ. Tính kim loại của các nguyên tố giảm dần.
Tính chất của các nguyên tố và đơn chất cũng như thành phần. Từ chu kì 4 trong mỗi chu kì. Hãy cho biết sự biến thiên tính kim loại và tính phi kim của các nguyên tố trong bảng tuần hoàn các nguyên tố.
Khi nói về sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học và định luật tuần hoàn. Sự biến đổi tuần hoàn cấu hình electron nguyên tử. Cấu hình electron nguyên tử có dạng.
Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học - hóa học 10Qua Bài giảng Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học và. Sự biến hóa tính sắt kẽm kim loại tính phi kim. Li Be B C N O F Ne.
Hóa trị của các nguyên tố - Trong cùng một chu kì đối với các nguyên tố nhóm A thì hóa trị biến đổi tăng dần từ I đến VII. Phát biểu đúng về X là. Số e lớp ngoài cùng của nguyên tử tăng dần từ 1 đến 8 electron.
- Tính kim. Phiếu học tập số 2 Câu 1. Từ bảng tuần hoàn các nguyên tố hóa học.
Câu hỏi trong đề. Hóa trị cao nhất của nguyên tố chính là. Sự biến đổi tính kim loại tính phi kim.
Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một nhóm A đựơc lặp đi lặp lại sau mỗi chu kì ta nói chúng biến đổi một cách tuần hoàn. Hydro là nguyên tố phổ biến nhất trong vũ trụ tạo nên khoảng 75 tổng khối lượng vũ trụ và tới trên 90 tổng số nguyên tử. Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học.
- Trong một chu kì từ trái sang phải theo chiều tăng dần của điện tích hạt nhân. Phương pháp giải bài tập về sự biến đổi tuần hoàn tính chất các nguyên tố hóa học đầy đủ ngắn gọn dễ hiểu. Định luật tuần hoàn.
Những tính chất biến đổi tuần hoàn của các nguyên tố. ĐỊNH LUẬT TUẦN HOÀN. A Nguyên tắc bố trí các nguyên ổn tố vào bảng tuần hoàn.
Các electron được phân bố vào phân lớp n-1d thuộc lớp ngoài cùng sau khi bão hòa phân lớp ngoài cùng ns 2. Sự biến hóa một số trong những đại lượng vật lý. Tính bazơ của các oxit và hidroxit tăng tính axit giảm dần.
1 Thủ Thuật Hướng dẫn Các đại lượng nào biến hóa tuần hoàn 2022. BẢng tuẦn hoÀn sỰ biẾn ĐỔi tuẦn hoÀn cẤu hÌnh electron cỦa nguyÊn tỬ vÀ tÍnh chẤt cỦa cÁc nguyÊn tỐ hoÁ hỌc. Sự biến đổi tính chất của các nguyên tố trong bảng tuần hoàn.
2022-05-03 110217Quý khách Cần tương hỗ về 1 anh chỉ hay mô tả ngắn gọn những nguyên tắc quản trị của Fayol. 2492161 là một cụm từ được yêu thích để hiểu được ý nghĩa của dãy số này bạn cần có một chút kiến thức về Hóa học và nắm được bảng tuần hoàn các nguyên tố trong Hóa học. Một nguyên tố X thuôc chu kì 4 nhóm VA trong bảng tuần hoàn.
Theo đó 24 là số hiệu nguyên tử của Crom Cr 92 là Uranium U 16 là Lưu huỳnh S. Đi từ trên xuống theo chiều tăng dần điện tích hạt nhân. Các sao thuộc dải chính được cấu tạo chủ yếu bởi hydro ở.
Bảng 24 Sự biến đổi tuần hoàn hóa trị của các nguyên tố ở chu kì 2 và 3 Nhận xét. Theo quy luật biến thiên độ âm điện trong bảng tuần hoàn nguyên tử của nguyên tố nào có độ âm điện lớn nhất không xét các khí hiếm. - Trong một chu kì theo chiều tăng của điện tích hạt nhân trong một nhóm theo chiều từ trên xuống dưới được lặp lại ở các chu kì khác nhóm khác theo cùng quy luật đó là.
Lý thuyết Hóa học 10 bài 9. Luyện tập tốc độ phản ứng và cân bằng hóa học. Định luật tuần hoàn.
Tính bazơ của các oxit và hidroxit tăng tính axit giảm dần. Kết luận. Bảng tuần trả sự chuyển đổi tuần trả thông số kỹ thuật electron ngulặng tử cùng đặc thù của các nguyên ổn tố hóa học.
Flo F là nguyên tố có độ âm điện lớn nhất 4 theo thang đo của Pauling. IV ĐỊNH LUẬT TUẦN HOÀN. Hóa trị cao nhất của một nguyên tố với oxi hóa trị với hiđro của các phi kim biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân.
- Trong 1 nhóm A. Số electron lớp ngoài cùng của nguyên tử các nguyên tố tăng dần từ 1 của Li đến 8 của Ne. Tính chất của các nguyên tố và đơn chất cũng như thành phần và tính chất của các hợp chất tạo nên.
2 Sự biến hóa tuần hoàn một số trong những tính chất của những nguyên tố. Chu kỳ 2 trong bảng tuần hoàn gồm 8 nguyên tố. Nhóm A bao gồm các nguyên tố.
Oxit cao nhất của một nguyên tố là RO2 trong hợp chất với hiđro có 25 hiđro về khối lượng. Chúng ta sẽ xét theo chu kì theo chiều tăng dần của điện tích hạt nhân và xét trong một nhóm theo chiều từ trên xuống dưới. Giải SBT Hóa học 10 Bài 9.
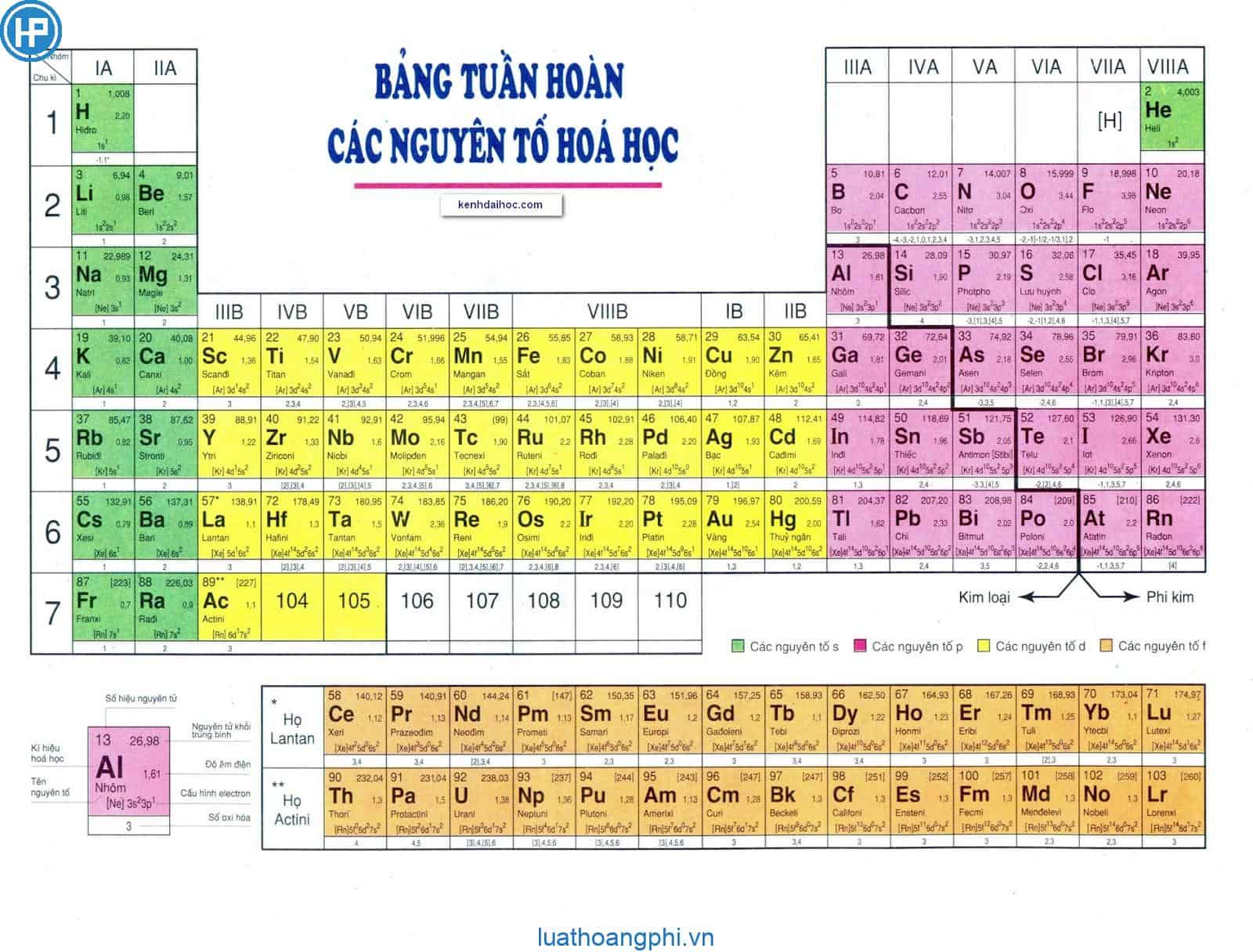
Bảng Tuần Hoan Cac Nguyen Tố Hoa Học Lớp 8 9 10
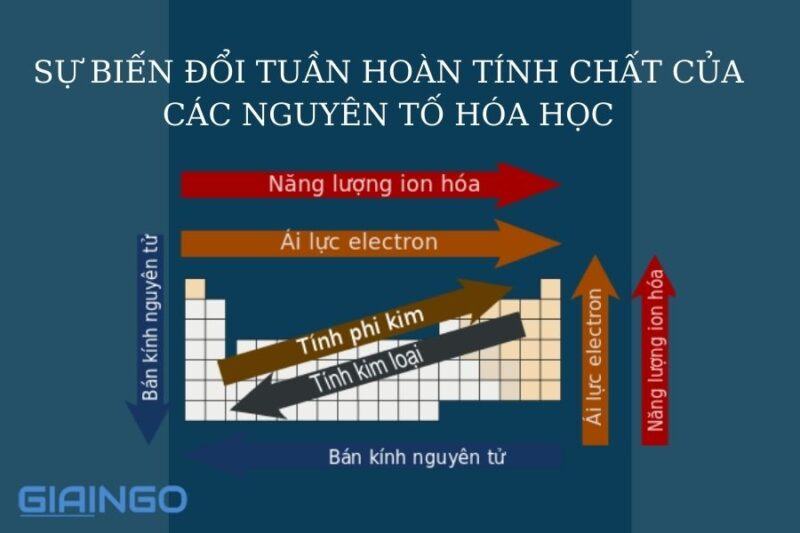
Sự Biến đổi Tuần Hoan Tinh Chất Của Cac Nguyen Tố Hoa Học
Chuẩn Nhất Nguyen Tắc Sắp Xếp Cac Nguyen Tố Trong Bảng Tuần Hoan Cac Nguyen Tố

